LEY DE BOYLE
DETERMINAR QUE PASA CON EL VOLUMEN SI SU PRESION AUMENTA Y
QUE PASA CON LA PRESION SI VOLUMEN AUMENTA
. La ley dice que: La presión ejercida por una fuerza química es inversamente proporcional a la masa gaseosa, siempre y cuando su temperatura se mantenga constante (si el volumen aumenta la presión disminuye, y si la presión aumenta el volumen disminuye).
 o
o 
 y
y 
. La ley dice que: La presión ejercida por una fuerza química es inversamente proporcional a la masa gaseosa, siempre y cuando su temperatura se mantenga constante (si el volumen aumenta la presión disminuye, y si la presión aumenta el volumen disminuye).
Matemáticamente se puede expresar esta relación inversa
entre presión y volumen como :
Cuando se reemplaza el símbolo de proporcionalidad, por un
signo igual y una constante de proporcionalidad, se ve que el producto de la
presión y el volumen de una cantidad fija de gas, a una temperatura dada, es
una constante ( ). El valor de a depende de la
cantidad de gas y de la temperatura. La ecuación
). El valor de a depende de la
cantidad de gas y de la temperatura. La ecuación  , se puede utilizar
para deducir otra ecuación útil cuando un gas sufre una transformación a
temperatura constante. Si escribimos la ecuación para un estado inicial (i) y
otro final (f), se obtiene :
, se puede utilizar
para deducir otra ecuación útil cuando un gas sufre una transformación a
temperatura constante. Si escribimos la ecuación para un estado inicial (i) y
otro final (f), se obtiene :
Como ambos productos  son iguales al mismo
valor de
son iguales al mismo
valor de  , se obtiene:
, se obtiene:
La ecuación anterior se usa para relacionar los cambios de
presión y volumen.
Para realizar sus experimentos con gases, Boyle utilizó un
tubo con forma de J. Una cantidad de gas queda atrapada en el tubo detrás de
una columna de mercurio. Boyle cambió la presión a la que estaba sometido el
gas agregando mercurio al tubo, y observó que el volumen del gas disminuía al
aumentar la presión.
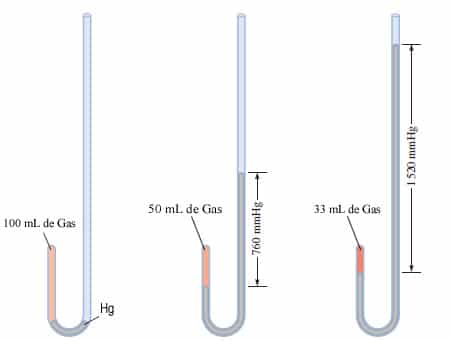
Para realizar sus experimentos con gases, Boyle utilizó un
tubo con forma de J
En la primera figura, los niveles del mercurio son iguales y
la presión del gas es igual a la presión atmosférica (760 mmHg). El volumen del
gas es de 100 mL. Al duplicar la presión mediante la adición de más mercurio,
el volumen del gas se reduce a 50 mL. Al triplicar la presión, el volumen del
gas disminuye a un tercio del valor original. La temperatura y cantidad del gas
se mantienen constantes.


Comentarios
Publicar un comentario